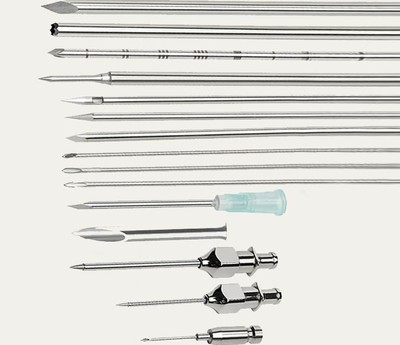
خط الأساس للسلامة: الامتثال التنظيمي ومراقبة الجودة وأنظمة إدارة المخاطر لإبر تشيبا
Apr 18, 2026
خط الأساس للسلامة: الامتثال التنظيمي ومراقبة الجودة وأنظمة إدارة المخاطر لإبر تشيبا
شروط المنتج الأساسية: اختبار التوافق الحيوي، التحقق من صحة التعقيم، ISO 10993، FDA 510(k)
الشركات المصنعة التمثيلية: جميع الشركات المصنعة الموجهة نحو السوق العالمية-مثل Cook Medical وBD، بالإضافة إلى الشركات المصنعة الصينية التي تسعى للحصول على شهادات دولية.
باعتبارها جهازًا طبيًا من الدرجة الثانية في معظم الولايات القضائية التنظيمية، تخترق إبرة تشيبا الجلد والأنسجة للوصول إلى جسم الإنسان، ولا تترك مجالًا للتنازل عن السلامة والفعالية. وبالتالي، بدءًا من المواد الخام وحتى استخدام المريض، تخضع دورة حياة المنتج بأكملها لرقابة تنظيمية صارمة وأنظمة إدارة الجودة. بالنسبة للمصنعين، لا يعد الامتثال مجرد مركز تكلفة؛ إنها رخصة العمل والشرط الأساسي لبقاء السوق.
I. الإطار التنظيمي العالمي
إشعار ما قبل التسويق لـ FDA 510(k) (الولايات المتحدة الأمريكية):تدخل معظم إبر تشيبا إلى السوق الأمريكية عبر المسار 510 (ك). يجب على الشركات المصنعة إثبات أن منتجها "يعادل إلى حد كبير" من حيث السلامة والفعالية "الجهاز الأصلي" الذي يتم تسويقه بشكل قانوني. ويتطلب ذلك تقديم وثائق فنية واسعة النطاق، بما في ذلك اختبار التوافق الحيوي، والتحقق من صحة التعقيم، واختبار الأداء. علاوة على ذلك، فإن لائحة نظام الجودة (QSR) الخاصة بإدارة الغذاء والدواء (FDA) تلزم الشركات المصنعة بإنشاء نظام لإدارة الجودة يغطي كل شيء بدءًا من التصميم وحتى أنشطة ما بعد السوق-.
لائحة الأجهزة الطبية في الاتحاد الأوروبي (MDR):يتطلب التسويق في الاتحاد الأوروبي الامتثال لـ MDR ووضع علامة CE. يتضمن هذا عادةً تدقيقًا بواسطة هيئة مُخطرة للتحقق من التوافق مع متطلبات السلامة العامة والأداء (GSPR) وإنشاء أنظمة مراقبة ومراقبة صارمة لما بعد-السوق.
تسجيل NMPA (الصين):في السوق الصينية، يعد التسجيل لدى الإدارة الوطنية للمنتجات الطبية (NMPA) إلزاميًا. تتضمن العملية اختبار المنتج، والتقييم السريري (غالبًا عبر المقارنة الأصلية للتجارب السريرية المستثناة)، وعمليات تدقيق نظام الجودة.
المعيار الدولي ISO 13485:هذا هو المعيار المعترف به عالميًا لأنظمة إدارة جودة الأجهزة الطبية. وهو بمثابة الأساس لدخول الأسواق العالمية، مع التركيز على إدارة المخاطر ومراقبة العمليات طوال دورة حياة المنتج.
ثانيا. نقاط مراقبة الجودة الأساسية: من المواد الخام إلى المنتج النهائي
تقييم التوافق الحيوي:تم إجراؤها وفقًا لمعايير سلسلة ISO 10993. باعتبارها جهاز اتصال خارجي ذو اتصال قصير المدى بالأنسجة، يجب أن تخضع إبرة تشيبا لاختبارات صارمة لسمية الخلايا، والحساسية، والتفاعل داخل الجلد للتأكد من أن المادة غير-سامة وغير ضارة.
التحقق من الأداء:
اختبار قوة الاختراق:يتحقق من حدة الإبرة عن طريق قياس القوة المطلوبة لاختراق الأنسجة المحاكية أو الوسيط القياسي.
اختبار الصلابة/المرونة:يوازن بين مقاومة الإبرة للالتواء أثناء الإدخال وقدرتها على التنقل في المسارات التشريحية المنحنية.
اختبار سحب المحور-إيقاف التشغيل: يضمن أن الاتصال بين المحور وقنية الإبرة يمكن أن يتحمل قوى الشد التي تواجهها أثناء الاستخدام.
التحقق من دقة المقياس: يضمن أن علامات العمق الموجودة على عمود الإبرة دقيقة ومقروءة للحصول على موضع دقيق للصورة-.
التحقق من صحة عملية التعقيم:عادةً ما يتم تعقيم إبر تشيبا التي تستخدم لمرة واحدة باستخدام أكسيد الإيثيلين (EO). يجب على الشركات المصنعة التحقق بدقة من درجة الحرارة والرطوبة وتركيز الغاز ووقت التعرض داخل غرفة التعقيم. تحديات التعقيم الروتينية باستخدام المؤشرات البيولوجية (على سبيل المثال،جيوباسيلس ستيروثرموفيلوسالجراثيم) إلزامية لإثبات أن العملية تحقق مستوى ضمان العقم (SAL) بمقدار 10⁻⁶.
التحقق من سلامة الحزمة:التغليف هو خط الدفاع الأخير عن الحاجز المعقم. يجب إجراء اختبارات مثل اختراق الصبغة، أو انبعاث الفقاعات (اختبارات التسرب)، أو اختبارات التحدي الميكروبي لإثبات أن العبوة تحافظ على عقم المنتج في ظل ظروف النقل والتخزين المحددة.
ثالثا. إدارة المخاطر واليقظة
إدارة المخاطر هي عملية مستمرة تمتد طوال دورة حياة المنتج بأكملها. يجب على الشركات المصنعة تحديد المخاطر المحتملة بشكل منهجي، مثل:
كسر طرف الإبرة:يتم التحكم فيه من خلال اختيار المواد الصارمة واختبار التعب.
إصابة الأنسجة أو النزيف: يتم تخفيفه من خلال تصميم الطرف الأمثل وتعليمات الاستخدام الواضحة (على سبيل المثال، التحذيرات ضد الاستخدام في مرضى التخثر).
عدوى: يتم التحكم بها من خلال التأكد من سلامة الحاجز المعقم وتقديم تعليمات للتعامل المعقم.
ثقب الأنسجة-غير المستهدفة: تم منع ذلك من خلال التأكيد على متطلبات الموضع الموجه للصور-.
يجب التحقيق في أي حدث سلبي يتم الإبلاغ عنه بعد-السوق، وإبلاغ السلطات التنظيمية به، ومعالجته من خلال الإجراءات التصحيحية والوقائية (CAPA) وفقًا لما يقتضيه القانون. على سبيل المثال، في عام 2024،كوك الطبيةبدأت فئة أذكرها لعدد محدد من إبر تشيبا نظرًا لاحتمال عدم كفاية قوة الختم، مما قد يؤدي إلى تعريض الحاجز المعقم للخطر. تؤكد مثل هذه الحوادث على الأهمية الحاسمة لنظام الجودة القوي والمراقبة اليقظة لما بعد-السوق.
رابعا. الآثار الاستراتيجية للمصنعين
بالنسبة للشركات متعددة الجنسيات مثل Cook Medical وBD، تعد الجودة الناضجة والأنظمة التنظيمية من الأصول الأساسية التي تدعم سمعة العلامة التجارية وحصة السوق. بالنسبة للمصنعين الصينيين الذين يطمحون إلى التوسع عالميًا، فإن إنشاء أنظمة جودة متوافقة مع ISO-يعد أكثر من مجرد "نقطة انطلاق" للأسواق الغربية؛ إنها عملية تفرض ترقيات الإدارة الداخلية وتعزز موثوقية المنتج بشكل عام. يتضمن ذلك رفعًا شاملاً للمعايير، بدءًا من إدارة غرف الأبحاث وضوابط الموردين وحتى التحقق من صحة العملية والتوثيق.
خامساً: الخاتمة: الجودة كمنتج للتصميم والإدارة
لا يتم تحقيق سلامة وفعالية إبرة تشيبا من خلال الفحص النهائي وحده. يبدأ الأمر باختيار المواد المتوافقة حيويًا، ويتم تحقيقه من خلال كل خطوة تصنيع يتم التحكم فيها بدقة، ويتم ترسيخه من خلال عملية تعقيم تم التحقق من صحتها بالكامل، ويتم ضمانه في النهاية من خلال نظام إدارة جودة سليم يمكن تتبعه. في صناعة الأجهزة الطبية، يشكل احترام التنظيم والالتزام الثابت بالجودة قدرة تنافسية أكثر ديمومة وجوهرية من أي تكتيك تسويقي. تحمل هذه الإبرة النحيلة وعدًا رسميًا بحياة المريض وصحته.